转录组测序在急性髓系白血病精准诊疗中的应用
转录组测序是指利用高通量基因测序技术对特定组织在某一状态下的所有信使RNA(mRNA)或包含mRNA在内所有基因转录产物进行测定。近年来,转录组测序在血液肿瘤中的应用越来越广泛,可以实现对基因融合、基因变异、基因表达及免疫基因多样性等生物标志物的检测,极大地拓展了对血液肿瘤分子机制的认识,以及推动血液肿瘤的诊断分型、预后分层和个体化治疗的精准化。莱顿大学医学院计算生物学研究中心的研究团队及其合作者于2021年在《Leukemia》杂志上发表了题为“Comprehensive diagnostics of acute myeloid leukemia by whole transcriptome RNA sequencing”的文章。该研究系统性评估了应用转录组测序技术来识别血液肿瘤相关多种类型遗传改变的可行性及准确性,为转录组测序技术的临床应用提供了重要的支持证据。

跟随小编一起来学习一下这篇经典的文献吧!
一、研究背景
急性髓细胞白血病(acute myelocytic leukemia,AML)是由一系列获得性遗传改变导致的一种血液系统肿瘤。2016年修订的WHO血液肿瘤分类,区分了9种携带重现性遗传改变且具有临床和预后特性的AML亚型。通过检测特定的遗传改变,可以对50-55%的AML患者进行风险评估,同时指导靶向治疗方案的选择。目前,AML的诊断需借助多种技术(如细胞遗传学、FISH或PCR)以实现对包括基因融合、基因变异在内的多种类型遗传变异的识别。因此,AML的临床诊断面临检测价高、复杂及不全面的困境。基于此,研究者探索利用转录组测序技术对AML进行一次性全面遗传改变识别的可能性。
二、研究设计
入组100例冷冻保存的AML样本,进行转录组测序,而后导入HAMLET生物信息学流程进行分析:利用STARFusion(version 0.5.4)& FusionCatcher(version 0.99.5a)识别RUNX1-RUNX1T1、CBFB-MYH11、PML-RARA、DEKNUP214等基因融合;基因变异(13个AML分型与预后相关基因:NPM1、FLT3、DNMT3A、ASXL1、 RUNX1、CEBPA、KIT、IDH1、IDH2 、TET2 、NRAS 、TP53和 WT1)的检出使用samtools mpileup (version1.3.1) 和VarScan (version 2.4.2);借助ReSCU(Reciprocal Soft Clip Utilization)算法进行FLT2和KMT2A的串联重复检测以及通过计算RPKM对基因的表达进行标准化。转录组测序检出的遗传改变均经常规方法(细胞遗传学、FISH、qPCR、PCR或NGS)进行了验证。
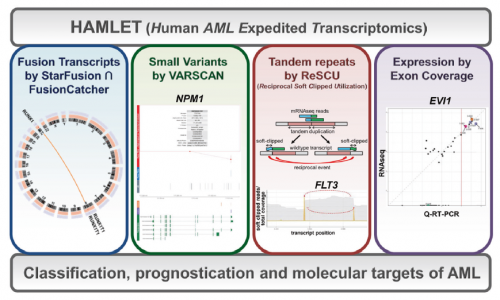
图一:HAMLET生信流程
三、研究结果
基因融合的检出
24例AML患者经细胞遗传学检测识别的基因融合均被转录组测序检出。转录组测序准确鉴别出发生11q23易位患者的KMT2A融合伙伴MLLT1、MLLT4和MLLT6。此外,转录组测序还额外检出8例细胞遗传检测阴性患者的基因融合:FUS-ERG(1例)、ETV6-LYN(3例)、NUP98-NSD1(1例)、PIM3-SCO2(3例)。转录组测序共检出54个细胞遗传学未检出的基因融合。

图二:全转录组测序检出基因融合
基因变异的检出
转录组测序在13个AML相关基因共检出246个变异,敏感性和特异性分别达到99.2%和100%。由于NGS测序大片段插入缺失识别存在一定限制,一个23bp ASXL1缺失和一个30bp CEBPA插入未能检出。所有转录组测序检出变异的类型和分布均与COSMIC数据库报告一致。
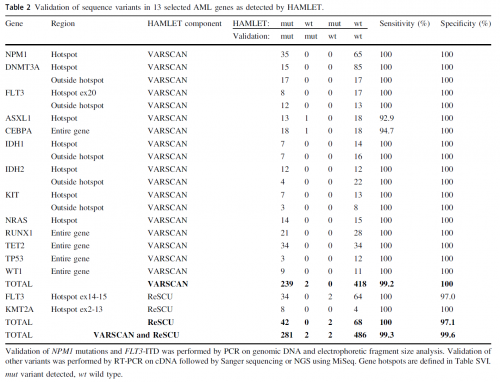
图三:转录组测序检出基因变异
串联重复的检出
FLT3串联重复(FLT-IDT)的检测具有重要的临床价值,其可指导FLT3抑制剂治疗。转录组测序共检出36例患者发生FLT3-IDT,其中34例患者经标准方法(NGS)证实。余下2例患者的NGS结果可观察到低于检测限(<1%)的FLT3-IDT信号,说明转录组测序较标准方法更灵敏。
KMT2A部分串联重复(KMT2A-PTD)是AML的不良预后分子标志物。转录组测序识别2-8外显子部分串联重复4例,2-10外显子部分串联重复2例,以及2、2-3和3-6外显子重复1例。9个KMT2A-PTD均经RT-PCR和测序验证。
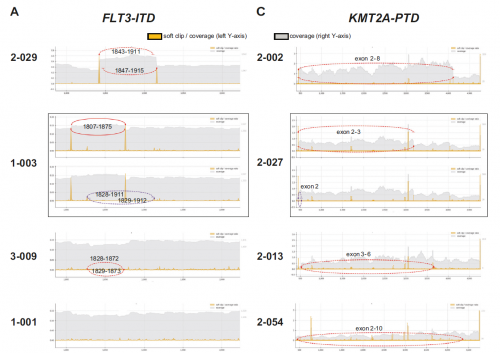
图四:RNA-seq检出FLT3和KMT2A串联重复
基因过表达的检出
正常基因的过表达会影响AML患者的预后,如EVI1、BAALC、ERG、MN1、DNMT3B和SPARC。EVI1的过表达可由inv(3)(q21q26)或t(3;3)(q21;q26)引起,但存在其他分子机制。转录组测序共检出8例EVI1高表达(log2 BPKM>0.1)患者,同时转录组测序与qPCR EVI1结果具有良好的相关性。
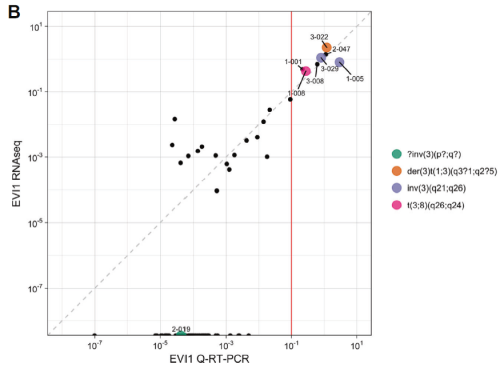
图五:RNA-seq与RT-PCR 检测EVI1表达
AML的分型及预后
在100例AML中,88例被诊断为具体的亚型,3例被诊断至亚群,9例未检出亚群分类标志物。在9例无分类的病例中,8例有可检测的驱动突变,1例未检测到驱动突变。图六中红色标出的为转录组测序可以检测而细胞遗传学未检出的遗传改变。

图六:100例AML的分子分型、风险评估及可用药靶点
四、总结
该研究表明转录组测序技术可以在一次检测中同时获得与AML预后和治疗相关的全面遗传信息,从而提升临床上对个体的预后评估及对靶向药物敏感性的预测,是促进AML精准诊疗有力工具。
参考文献
Comprehensive diagnostics of acute myeloid leukemia by whole transcriptome RNA sequencing. Leukemia. 2021 Jan;35(1):47-61. doi: 10.1038/s41375-020-0762-8.Epub 2020 Mar 3. PMID: 32127641; PMCID: PMC7787979.
OC209:血液肿瘤转录组测序
迈基诺自主研发适用于急性髓系白血病、急性淋巴细胞白血病、淋巴瘤等血液系统肿瘤的转录组测序项目,基于高通量测序技术,准确检测血液肿瘤相关的基因融合和基因突变,可满足临床诊断及鉴别诊断、预后判定和指导治疗的具体需求。
|
血液肿瘤 |
诊断及鉴别诊断 |
预后判定 |
指导治疗 |
额外价值 |
|
AML |
NPM1、CEBPA、RUNX1 |
KIT、FLT3、NPM1、CEBPA、IDH1/2、TP53、RUNX1、ASXL1、DNMT3A、SF3B1、U2AF1、SRSF2、ZRSR2、EZH2、BCOR、STAG2 |
FLT3、IDH1/2、NPM1、KIT |
发现新的诊断及鉴别诊断、预后判断和指导治疗标志物 |
|
ALL |
|
IKZF1、TP53、NOTCH1、FBXW7 |
ABL1、JAK3、JAK1 |
|
|
MPN |
JAK2、CALR、MPL、CSF3R、ASXL1、EZH2、TET2、IDH1/2、SRSF2、SF3B1 |
JAK2、CALR、MPL、ASXL1、EZH2、IDH1/2、SRSF2、TP53、SH2B3、SF3B1、U2AF1、ABL1 |
JAK2、CSF3R、ABL1 |
|
|
MDS |
SF3B1、TET2、ASXL1、DNMT3A、SRSF2、RUNX1、TP53、U2AF1、EZH2、ZRSR2、STAG2、CBL、NRAS、JAK2、SETBP1、IDH1/2、ETV6 |
ASXL1、EZH2、SF3B1、SRSF2、U2AF1、ZRSR2、RUNX1、TP53、STAG2、NRAS、ETV6、SETBP1、BCOR、FLT3、WT1、STAT3 |
TET2、STAT3、TP53 |
|
|
B细胞淋巴瘤 |
TP53、MYD88、BRAF、MAPK1、CXCR4、TCF3、ID3、BCL6、MAP2K1、NOTCH2、KMT2D、KLF2、SPEN |
TP53、SF3B1、ATM、BIRC3、NOTCH1/2、KLF2、BCL6 |
TP53、BTK、PLCG2、NOTCH1、SF3B1、BIRC3、MYD88、CXCR4、BCL6、BCL2 |
|
|
T/NK细胞淋巴瘤 |
STAT3、STAT5B、ATM、JAK1 |
STAT5B |
|
|
|
项目编号 |
项目名称 |
检测内容 |
检测方法 |
检测周期 |
样本类型 |
|
OC209 |
血液肿瘤转录组测序 |
基于高通量测序技术,准确检测血液肿瘤相关的基因融合和基因突变,可满足临床诊断及鉴别诊断、预后判定和指导治疗的具体需求。 |
NGS |
14个自然日 |
骨髓液或外周血 |
 健康教育网
健康教育网












